Escrito por Bernardita Sallato, WSU Tree Fruit Extension Specialist. Junio 2021.
Para leer la versión en Inglés, visite Leaf Tissue Analysis
Introducción
El análisis elemental de tejidos foliares es una de las herramientas más utilizadas y estandarizadas para el diagnóstico de nutrientes y manjejo nutricional de huertos. Para poder utilizar el análisis foliar en forma efectiva, es importante entender cómo tomar las muestras y qué nos informa un análisis foliar.
Qué nos indica el análisis foliar
- Qué elementos están o no en concentración adecuada, deficiente o en exceso (Marschner 2002, Hart et al. 1997).
- Qué nutrientes fueron absorbidos por la planta o tejido.
Qué NO nos indica el análisis foliar
- El porqué de deficiencia o toxicidad.
- Cuánto debo aplicar.
- Qué producto aplicar.
Por lo tanto, el análisis foliar es una herramienta util para guiar y monitorear los nutrientes en las plantas, identificar si existen problemas de absorción o determinar excessos. Para obtener mayor informacion respecto a los manejos que deben realizarse antes problemas de deficiencia o toxicidad, el análisis foliar debe ser complementado con otras herramientas de análisis: como análisis de suelos, historial del huerto, manejos de riego, entre otros.
Cómo interpretar un análisis foliar
Para poder interpretar adecuadamente un análisis foliar, los resultados deben ser comparados con los valores estándares para la especie, o en caso del diagnóstico de problemas, fuera de la época estándar, se recomienda comparar entre sectores del huerto que presenten diferencias, ejemplo; sector clorótico versus sector más verde.
Uso de estándares: El uso de estándares nos permite comparar los valores obtenidos con valores cientificamente validados (Tabla 1). Para ello, es fundamental seguir las recomendaciones de toma de muestras, respecto a la edad y tipo de tejido a muestrear.
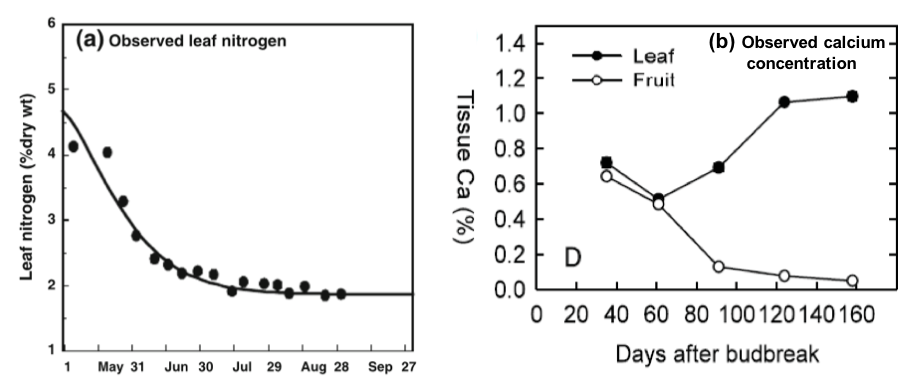
Los estándares fueron desarrollados para utilizar como referencia, considerando con qué concentración de nutriente en la hoja se optiene el máximo potencial productivo. Dado que la concentración de nutrientes en las hojas varia con la edad y el elemento (Figura 1). Los estándare nutricionales se establecieron de manera que proporcionen un valor estable y a la vez sensible. La estabilidad de los nutrientes se obtiene una vez que la hoja alcanza madurez (o su tamaño completo). Como se observa en la Figura 1. Los niveles de N parte siendo alto (mayor a 4%), y declina a medida que la hoja madura y adquiere mayor biomasa, por lo que se diluye y llega a valores adecuados de 1.5 a 2.5 en plena madurez (Figura 1, derecha). El Ca por el contrario, parte con niveles bajos en las hojas y aumenta a medida que la hoja madura (Figura 2, izquierda). Notese que el Ca en la fruta tiene un comportamiento opuesto al de la hoja, disminuyendo en concentración una vez que el fruto madura. La estabilidad es fundamental para que sea una herramienta confiale y práctica, ya que necesitamos tener un valor que sea representativo y no susceptible a cambios de clima o agua.
El análisis de savia (sap) que se ha popularizado en los últimos años puede ser una herramienta últil para hacer seguimiento de la variación de nutrientes en las plantas, con propositos de investigación especialmente, sin embargo, los nutrientes en especies perennes (manzanos, cerezos, perales, etc.) es muy variable e inestable, por lo tanto no se han desarrollado estándares en fruticultura. La ausencia de estándares científicos ha prevenido el uso de la técnica para el manejo rutinario de fertilización en huertos, ya que los valores no se pueden associar con toxicidad o deficiencia.
En contraste, la toma de muestras de tejidos foliares ya se encuentra validado como indicador del estado nutricional de las plantas, además de ser bastante economico, demonstrando un buen compromiso entre eficiencia y efectividad. Dado que los nutrientes se estabilizan cuando la hoja alcanza madurez, se recomienda que la toma de muestras se realize durante inicios de verano, de hojas ubicadas generalmente en el medio de la ramilla o dardo sin frutos, (Figura 2). En la Tabla 1. se indican el rando de valores recomendados para diferentes especies frutales.
Tabla 1. Estándares nutricionales en tejidos foliares.
| Nutriente | Unidad |
Manzanoa,c,d,e | Peraa,c,d,e | Cerezob | Duraznob | Damascoa,b |
| Nitrógeno (N) | % | 1.7 – 2.5 | 1.8 – 2.6 | 2.00 – 3.03 | 2.7 – 3.5 | 2.4 – 3.3 |
| Fósforo (P) | % | 0.15 – 0.3 | 0.12 – 0.25 | 0.10 – 0.27 | 0.1 – 0.30 | 0.1 – 0.3 |
| Potasio (K) | % | 1.2 – 1.9 | 1.0 – 2.0 | 1.20 – 3.3 | 1.2 – 3.0 | 2.0 – 3.5 |
| Calcio (Ca) | % | 1.5 – 2.0 | 1.0 – 3.7 | 1.20 – 2.37 | 1.0 – 2.5 | 1.10 – 4.00 |
| Magnesio (Mg) | % | 0.25 – 0.35 | 0.25 – 0.90 | 0.30 – 0.77 | 0.25 – 0.50 | 0.25 – 0.80 |
| Azufre (S) | % | 0.01 – 0.10 | 0.01 – 0.03 | 0.20 – 0.40 | 0.2 – 0.4 | 0.20 – 0.40 |
| Cobre (Cu) | mg/Kg | 5 – 12 | 6 – 20 | 0 – 16 | 4 – 16 | 4 – 16 |
| Zinc (Zn) | mg/Kg | 15 – 200 | 20 – 60 | 12 – 50 | 20 – 50 | 16 – 50 |
| Manganeso (Mn) | mg/Kg | 25 – 150 | 20 – 170 | 17 – 160 | 20 – 200 | 20 – 160 |
| Hierro (Fe) | mg/Kg | 60 – 120 | 100 – 800 | 57 – 250 | 120 – 200 | 60 – 250 |
| Boro (B) | mg/Kg | 20 – 60 | 20 – 60 | 17 – 60 | 20 – 80 | 20 – 70 |
Adaptado de:
a Shear and Faust, 1980;
b Reuter and Robinson, 1997;
c Righetti et al., 1990;
d Silva and Rodriguez, 1995;
e Penn State University, based on July-August sampling of mature leaves.
Estos estandares han demostrado ser correctos para differentes cultivares, portaijertos y condiciones ambientales. Para el caso de ´Honeycrisp´ el Profesor Dr. Cheng recomienda manejar el cultivar dentro de los niveles más bajos del rango adecuado para N y K.
Comparación de muestras en caso de diagnóstico fuera de la época estándar: En caso de evaluación de casos especiales, como cuando se quiere diagnosticar un problema, sin embargo nos encontramos fuera de la época en la cual podemos usar los estándares indicados previamente, se puede realizar el análisis foliar en forma comparativa, utilizando sectores diferenciados del huerto. En éste caso, es importante estandarizar la toma de muestras para comparar entre el mismo cultivar, edad, suelo, posicion en la ramilla, tratando de reducir al máximo interferencia de factores. Además, en caso de problemas en las cuales las plantas presentan síntomas severos, el análisis elemental del tejido foliar puede ser confuso de interpretar o irrelevante.
Additionally, under comparative circumstances or experimental trials, other complementary analyses as sap analyses, such fruitlets and soil chemical analyses should be utilized for an integrated analysis.
Toma de muestras
Tome muestras siguiendo protocolos asociados a la especie. Para la mayoría de las especies frutales, se debe seleccionar hojas recientemente maduras del tercio medio de la ramilla del año (o dardo nuevo), en ramillas sin frutos. En Washington, generalmente este tejido se encuentra entre Julio y mediados de Agosto. (Figura 2). Para el caso de ´Honeycrisp´ Dr. Cheng recomienda tomar las muestras foliares antes de que aparezca la clorosis intervental.

Asegurese de tomar muestras que sean representativas de la ramilla, el árbol y el huerto. Tome 50 hojas por sector de muestreo (máximo 10 acres por sector), desde sectores homogeneos. No mezcle muestras de diferentes especies, cultivares, edad, suelo o manejo de riego. Evite muestras de ramillas muy viejas o vigorosas, o muy deviles que no representen bien la condición del huerto. Evite hojas que tengan suciedad como fecas de pájaro o insectos. Se aconseja muestrear al menos 15 días después de la última aplicación de pesticidas o fertilizantes, ya que algunos pesticidas contienen micronutrientes como Zn, Cu, S, Ca o B. Si no es posible, se debe advertir al laboratorio de análisis y tomar en consideración el momento de interpretar los resultados.
Las muestras de deben colocar en bolsa de papel para evitar transpiración y condensacion de agua dentro de la muestra. Se aconseja mantenar en cooler o en la sombra, y una vez que tenga las muestras bien identificadas, enviar en forma inmendiata al laboratorio, dentro de 24 horas.
Dónde enviar las muestras?
Existen varios laboratorios acreditados en el estado de Washington y Oregon. Verifique que el laboratorio utilize métodos acreditados y validados los que puede encontrar en este link, y que el laborio participe en las rondas de proficiencia del programa North American Proficiency Testing (NAPT). Este programa es manejado por la Soil Science Society of America y ayuda a los laboratorios químicos en la evaluación de sus métodos de análisis y proficiencia. La lista de laboratorios acreditados se actualiza anualmente y se puede encontrar en este link (Accredited laboratories for 2022).
Análisis recomendados
Un análisis completo incluye : Total N, P, K, S, B, Ca, Mg, Zn, Mn, Cu, Na.
Dependiendo del tipo de suelo, hay análisis que son más importantes que otros. Por ejemplo, en caso de bajo pH de suelo (suelo ácido) el análisis de metales de aluminio (Al) puede ser relevante. En condiciones de alta salinidad, se puede incluir cloro (Cl). El análisis total de hierro (Fe) aunque se inclute en los análisis completos, no es un buen indicador de deficiencia.
Guía de interpretación del resultado foliar
Table 2. When nutrients are out of the adequate range, assuming correct tissue sampling procedure and adequate laboratory analyses.
| Nutriente | Resultado | Consideraciones |
Recomendación |
| Nitrogeno (N) | Alto | Si tiene exceso de vigor, crecimiento | Reduzca la dosis de N |
| Si observa bajo crecimiento o vigor |
Verifique otros factores como riego, luz, salinidad, patógenos |
||
| Bajo | Si presenta bajo vigor y clorosis | Aumente la dosis de N | |
| Si tiene excesivo vigor | Reduzca la dosis de N | ||
| Fósforo (P)
Potasio (K) Calcio (Ca) Magnesio (Mg) Azufre (S) |
Alto | Si está alto en el suelo | Reduzca la dosis, verifique programa de fertilización |
| Si está bajo en el suelo |
Puede asociarse a aplicaciones recientes foliares
Verifique contaminación de muestras |
||
| Bajo | Si se encuentra alto en el suelo | Se debe a problemas de absorción en las raíces. Verifique pH, agua, patógenos, u otros. | |
| ISi se encuentra bajo en el suelo | Aumente la dosis de fertilización | ||
| Boro (B)
Zinc (Zn) Cobre (Cu) |
Alto | Si está alto en el suelo | Reduce or suspend fertilization |
| Si está bajo en el suelo | Reduce or suspend sprays
Verify contamination/ presence in sprayed products |
||
| Bajo | Alto en el suelo | Verifique pH – suelos alcalinos (pH > 7), guiese por el análisis o síntoma visual | |
| Bajo en el suelo | Corregir en el suelo y complemente con aplicaciones foliares | ||
| Manganeso (Mn) | Alto | Alto en suelos |
Verifique condición de humedad del suelo y drenaje. Bajo anoxia, Fe y Mn se hace más disponible. |
| Bajo en suelos | Verifique su programa de aplicación foliar Verifique contaminación |
||
| Bajo | Alto en suelos | Verifique pH – en suelos alcalinos (pH > 7). Maneje con fertilizante foliar | |
| Bajo en suelos | Corregir nieveles en el suelo, complemente con aplicación foliar. | ||
| Hierro (Fe) | Alto o Bajo | – | Hierro total no es un buen indicador de deficiencia. Es preferible verificar síntomas de clorosis. |
La información entregada es información general que puede usarse como guía de interpretación. Para desarrollar un programa nutricional, se recomienda integrar con análisis de suelos, historial del huerto y sintomatología.
Contacto
Bernardita Sallato
WSU Tree Fruit Extension Specialist
Prosser-IAREC
b.sallato@wsu.edu
Referencias
Crassweller, R. It’s Time to Evaluate the Nutritional Status of Fruit Trees. Web page link
Cheng, L. and R. Raba. 2009. Nutrient Requirement of Gala/M.26 Apple tree for high yield and quality. Cornell University.
Hardman J.M., W. Van der Werf, S. Blatt, J. Franklin, R. Karsten and H. Teismann. 2013. Simulating effects of environmental factors on biological control of Tetranychus urticae by Typhlodromus pyri in apple orchards. Experimental & Applied Acarology. 60. 10.1007/s10493-012-9640-z.
WSU Tree Fruit Extension articles may only be republished with prior author permission © Washington State University. Reprint articles with permission must include: Originally published by Washington State Tree Fruit Extension at treefruit.wsu.edu and a link to the original article.

